Experiment des Monats
August 2003
Zinksulfid


|
Experiment des Monats
|

|
Die Bildung von Zinksulfid aus den Elementen ist eine stark exotherme Reaktion. Der Reaktionsverlauf ist sehr spektakulär, allerdings ist dieser Versuch nicht ganz ungefährlich und daher nur für geübte Experimentatoren geeignet.
 |
 |
 |
 |
Geräte und Chemikalien:
Zink-Pulver,
Schwefel
Erlenmeyerkolben, Porzellanschale, Eisendraht.
Durchführung:
4 g Zinkpulver und 2 g Schwefel in einem trockenen Kolben
durch Schütteln vermischen. Das Gemisch in einer flachen Porzellanschale
(Kachel, Metallschale) aufschütten und auf eine feuerfeste Unterlage stellen.
Im Umkreis von 1-2 m dürfen sich keine brennbaren Substanzen befinden!
Gezündet wird am besten mit einem glühenden dicken Draht
(Stricknadel, Fahrradspeiche etc. in einem Bunsenbrenner zum Glühen bringen).
Sicherheitshinweise beachten!
Beim Berühren des Gemischs mit dem glühenden Draht schmilzt
zunächst etwas Schwefel. Dann beginnt die Reaktion unter
Flammenerscheinung und Bildung von weißem Rauch.
Die Reaktionsprodukte erscheinen zunächst hellgelb, nach dem Abkühlen
weiß-hellgrau. Verantwortlich dafür ist das an der
Oberfläche gebildete Zinkoxid, das Thermochromie zeigt.
Eine Probe des entstandenen Zinksulfids kann (im Abzug!!)
mit verd. Salzsäure übergossen und der entstehende
Schwefelwasserstoff (H2S,
giftig!)
mit Bleiacetatpapier nachgewiesen werden.
Erklärung:
Zwischen den beiden Elementen läuft eine Redox-Reaktion ab.
Zink wird oxidiert, Schwefel reduziert. Die Reaktion ist stark
exotherm.
Zn + S 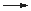 ZnS
ZnS
Teilweise erfolgt eine Oxidation des Zinks durch Luftsauerstoff zu Zinkoxid (ZnO), außerdem können (durch Reaktion mit Sauerstoff bzw. Wasser) SO2 und H2S entstehen.
Gefahren:



Das Zink-Schwefel-Gemisch ist explosiv! Nur vorsichtig
und ohne Druck mischen. Nur kleine Mengen verwenden.
Das Experiment darf nur unter entsprechenden
Sicherheitsvorkehrungen durchgeführt werden.
Schutzbrille oder besser Gesichtsschutz tragen und
eine Sicherheitsscheibe aufstellen!
Die zündende Hand mit einem feuerfesten Schutzhandschuh
oder Leinentuch schützen.
Da giftige Nebenprodukte (u.a. H2S)
entstehen, den Versuch am besten im Abzug durchführen.
Die glühenden Schwefel/Sulfid-Spritzer verursachen
auf der Haut schwere Verbrennungen! Daher auf ausreichenden
Sicherheitsabstand achten. Keine brennbaren Stoffe in der
Nähe lagern.
Entsorgung:
Die Rückstände zum Schwermetall-Abfall geben.
Literatur & Links:
F. Bukatsch, W. Glöckner: "Experimentelle
Schulchemie", Bd. 3 - Versuch 241, S. 141
F. Bukatsch, O. Krätz, G. Probeck, R. Schwankner: "So interessant
ist Chemie" - Versuch 72, S. 83-84
F. R. Kreißl, O. Krätz: "Feuer und Flamme,
Schall und Rauch" - V. 9.3, S. 89-90
H. W. Roesky, K. Möckel: "Chemische
Kabinettstücke" - V. 92, S. 221-222
Am Computer-Chemie-Centrum ist zu diesem Versuch ein Video verfügbar.
Dipl.-Umw.Wiss. Simon Spycher und Dipl.-Chem. Rastislav Krajcik danke ich sehr herzlich für die Mitarbeit.
Juli 2003: Eine endotherme Reaktion
 zurück zum aktuellen Experiment
zurück zum aktuellen Experiment
Seite erstellt am: Donnerstag, 31. Juli 2003, A. Schunk, CCC Univ. Erlangen.
Für den Inhalt externer Seiten wird keine Verantwortung übernommen!